|
编者的话:美国财富杂志3月22日发表一位癌症患者经过长时间调研后发表的文章,披露了美国癌症研究领域存在的诸多问题,并提出了相应的解决方案。
这些问题值得我国学术界及政府管理部门关注。今天同时刊登摘译的上、下两部分。
Avastin、Erbitux、Gleevec…,当美国食品药物管理局一改多年常规,加速批准抗癌新药以来,已经有一连串的抗癌新药上市。看起来,人类正在抗癌大战中赢得胜利。然而事实并非如此。
特别关注:抗癌大战人类如何才能获胜?(上)
毫无感恩之意的问题
奇怪的是当年那股怪味我仍然记忆犹新。那是在1978年,我刚过15岁生日不久。我悄悄潜入我哥哥的卧室,那靠墙顶到天花板的书架上放着我们家最笨重的书籍:24卷大英百科全书。红褐色的书脊上覆盖了一层土,打开书,一股怪味扑鼻而来,就像是发霉的旧枕头抹上了一层薄荷。我小心翼翼地打开有何杰金氏病的那一卷,厚重的书放在我的膝盖上,就像是一部圣经。阅读那几段关于何杰金氏病的文字要花很长时间。那些有关“淋巴系统”、“肉芽肿”、伽马射线的叙述显得很神秘,就像是何杰金氏病一样令人费解。大夫刚刚告诉我,我得了这种病,像是科幻电影里发生的事情。不过书上最后那一句话我能彻底理解:75%%的何杰金氏病患者会在5年内死去。
结果我很幸运,没有死去。虽然癌细胞已经从我的脖子扩散到肺以及脾,医生动手切除了我的脾脏,化疗、放疗使我的头发几乎脱光,但是我很幸运地参与了全国癌症研究院的临床试验,那是试验一种疗法,四种有毒化学药物联合使用,名为MOPP,再加上放疗,所有的医疗费由纳税人负担。我总算活下来了。在有了这样一番经历以后,我要提出的问题听起来毫无感恩之意:为什么我们在抗癌大战中进展甚微?
提出这样的问题也许令人吃惊。我们不是在抗癌领域不断取得进展吗?最新见诸报端的抗癌新药如Gleevec、Herceptin、Iressa、Erbitux,还有刚刚批准的Avastin,征服癌症的前景似乎近在眼前。
可是事实并非如此。期望及乐观,这是癌症病人抗癌的必备要素。然而这种期望及乐观掩盖了非常现实的一系列问题:癌症是非常复杂的疾病,病因不明,要征服癌症极其困难。从1971年颁布国家癌症条例开始抗癌大战以来,一方面我们已经取得相当多的成果,另一方面距离抗癌大战的胜利仍然非常遥远。迄今为止,看起来,我们像是正在输掉这场战争。
严酷的统计数字
我们还是来统计一下战场上的牺牲者吧。2004年,将有563700位美国人死于癌症,未来14个月里死于癌症的美国人人数将超过美国历史上死于战争人数的总和。尽管过去30年中,研究及医疗领域的工作大大加强了,相关经费投入也大幅上升,然而每年因癌症死亡人数却上升了73%%,这一上升速度是美国人口增长速度的1.5倍。
在未来10年中,癌症将取代心脏病成为美国人的头号杀手,这是美国国家癌症研究院及疾病控制中心的预测。对于75岁以下的美国人,癌症已经是头号杀手。在45-64岁的人群中,癌症致死人数超过后三大死因(心脏病、意外事故及中风)致死人数的总和;在幼儿到30岁的年龄段,癌症也是第一大杀手。
研究人员指出,人类的平均寿命延长,随着年龄的增长,癌症发病率也增长,所以如果仅以原始数据来评判抗癌的进展,不太公平。在测算癌症致死率时,研究人员对不同时代同一年龄段的人群进行比较,以对统计结果进行修正。就算是采用这样的分析方法,现在死于癌症的美国人占美国人口的比例与上一世纪七十年代甚至上一世纪五十年代大体相同。如果把癌症与另两大杀手心脏病、脑血管意外相比,结果更令人震惊:同样采用年龄因素修正法进行统计,心脏病致死人数占美国人口比例同期下降了59%%,中风致死人数占美国人口比例50年来下降了69%%。
研究人员还认为,癌症病人的生存期比过去延长了。这方面的统计更令人失望:癌症病人生存期的延长是以月而不是年计算的。少数治愈率或是患者生存期得到大幅提高的癌症往往发病率不高,如何杰金氏病及白血病等。33年前,从癌症确诊以后存活5年及5年以上的美国人占美国癌症患者总数的50%%,现在这一数字仅提高到63%%。
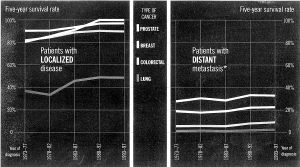
在这小幅增长中,能够归功于国家癌症研究院的实验室或是大型癌症研究中心发现的那些新型抗癌化合物的部分少而又少,而这些实验室及研究中心是大笔公共经费的主要去处。相反,人们行为的简单变化如戒烟有效地减少了肺癌的发病率;更重要的是,利用乳房自检及乳房造影术,检测前列腺癌的PSA测试法以及其它检测手段,我们能够早期发现癌症。RuthEtzioni是西雅图FredHutchinson癌症研究中心的生物统计学家,他指出,如果把4大癌症(肺癌、肠癌、乳腺癌及前列腺癌)按照患者确诊癌症时的不同阶段细分(即医学上根据癌细胞是否扩散或扩散程度分为4期),那么33年来存活5年的中晚期癌症转移患者在癌症患者总数的比例几乎没有变化。(见附图)
另一方面是新的癌症患者不断出现。在上一世纪七十年代抗癌大战开始以来,癌症患者人数不断上升,只有九十年代中期有所下降。今年又将有140万美国人同他们的医生进行那番令人胆战心惊的谈话并加入癌症患者的队伍。每两位男士中有一位、每三位女士中有一位在一生中会罹患癌症。有一位研究人员总结说:“这就像是每天都发生一次世贸大厦坍塌事件。”
问题产生了:为什么我们没有在这场持续数十年的抗癌大战中获胜?我们现在做什么才能扭转这种被动局面?
抗癌大战就像希腊悲剧
在三个月的采访中,我奔波于休斯顿、波士顿、纽约、华盛顿以及其它癌症研究机构集中的地区,采访了数十位在一流癌症医院工作的研究人员、医生、流行病学家,在制药公司及癌症研究中心工作的药理学家、生物学家、遗传学家,食品药物管理局、国家癌症研究院、国家卫生研究院的官员,还有资金筹集人、癌症患者、社会活动家等等。我向他们提出上述问题。我得到的大多数回答都是对现在取得的进展表示乐观,大家认为,严酷的统计数字掩盖了我们已经获得大量知识的真相,而这些知识宝藏将引导我们在未来找到针对癌症的有效疗法,癌症是我们对100余种疾病的总称。大多数人认为,尽管他们经常对研究方式产生疑虑,但是感觉走的路还是对的。
如果把所有这些专家提供的证词综合起来,实际上可以描绘出一种有问题的“癌症文化”,就是一种集团思维方式,在这种思维方式驱动之下,成千上万的医生及科学家都为寻求癌症治疗的点滴改进而奋斗,却不是追求真正的突破;这种思维方式导致各自为战,重复研究,而不是合作;这种思维方式把学术成果及论文发表放在至高无上的位置。
从基础研究到临床的每一步,研究者都依赖那些预测成功率非常低的模型,结果是数百种药物投入试验,有许多药物获得FDA的批准,而实际上那些药物“经过验证”的药效同癌症治疗基本不相关。英特尔公司主席葛洛夫是一位前列腺癌患者,他多年来作为几家癌症咨询团体的成员,一直设法改变这种“癌症文化”。他的结论是:“这就像希腊悲剧,每个人就他自身而言都做得尽善尽美,每个人从他一生而言所作所为无懈可击,然而总体却不成功。”
不幸的是,悲剧这个词对于癌症文化太贴切了。英雄们徒劳地同比他们强大得多的势力搏斗,导致不必要的死亡及毁灭。不过与希腊悲剧不同,希腊悲剧是命运注定结局,而抗癌大战却不是非要如此进行,而且它不应该继续这种悲剧方式。
癌症杀手擅长变异
1939年9月,德国战车开进波兰,第二次世界大战开始了。此时核裂变这一新词只有8个月的生命。物理学家玻尔在乔治华盛顿大学的一次理论物理学术会议上首次发布了他的这一发现。三年以后,基于核裂变原理开发原子弹的曼哈顿计划开始运行。又过了三年,1945年8月6日,一颗名为小男孩的原子弹在日本广岛上空爆炸。
美国航空航天局是1958年10月1日成立的。11年以后,两位美国人登上月球。绘制人类基因图谱的研究也就进行了18年,最早是科学家们在加州SantaCruz召开的一次小型学术会议上提出这一想法的。就算是追溯到Watson与Crick破解DNA结构的年代,也就是半个世纪。
从事癌症研究的科研人员不愿意做这样的比较。许多癌症研究人员认为,癌症研究不同于曼哈顿计划、火箭科学甚至遗传学研究,很难人为设定目标。
可以肯定的是,癌症的挑战同上述那些大科学计划完全不同。原因是癌症杀手太擅长变化了。费得勒是休斯顿M.D.Anderson癌症中心癌生物学部的主任,他指出:癌细胞的特点就是其遗传学不稳定性。癌细胞的DNA不同于正常细胞的DNA,正常细胞分裂时,其遗传信息被完美无缺地复制到下一代细胞;而癌细胞分裂时,复制到后代的遗传信息却会改变,而且遗传信息的细微变化会导致癌细胞行为的显著变化。结果就是当人们认为某种癌细胞是同一种细胞的时候,实际上这种癌细胞已经分化出难以计数的不同细胞,构成一个癌细胞大家族,这些癌细胞各有各的特点,诡诈无比。费得勒说:“癌细胞的这种非一致性是最主要的障碍,它阻碍人们找到针对癌症的简易疗法。”
纽约市MemorialSloan-Kettering癌症中心的主任瓦穆斯(HaroldVarmus)也赞同这一观点。瓦穆斯因发现第一种致癌基因而分享了1976年的诺贝尔医学奖,他的研究成果为基因变异导致癌症的理论奠定基础。他在克林顿政府期间出任国家卫生研究院院长,任职期间癌症研究经费大幅增长。他说:“这是一组非常难解的问题。我们回头看总是觉得时间很短。30年间,人类从几乎对癌症成因全然无知到积累了大量知识。”
然而知识的积累是付出了巨大代价的。不同的观点主要是针对代价:我们为获得这些知识付出的代价是否过于高昂?
尼克松总统在1971年国情咨文中用了大约100个词建议开展深入的研究以寻找治疗癌症的方法。他当时并没有用“战争”这个字眼。在尼克松国情咨文到12月签署国家癌症条例(theNationalCancerAct)这段时间里,两派关于是要“创造性研究”还是“组织研究”争论甚嚣尘上,核心问题是组织癌症研究的国家机构究竟应当拥有多大权力。作为争论的一方,医学学术组织、医学院校以及当时的三大癌症医院(上面提到的MemorialSloan-Kettering,M.D.Anderson,及布法罗的RoswellPark)结成广泛同盟,他们乐于接受来自联邦政府的资助,但不愿接受政府的指导甚至哪怕是松散的协调。
争论的另一方是被公认为癌症研究教父的波士顿医生西德尼・法伯(SidneyFarber),他认为应当开展大规模、有组织的研究。他当时说:“我们不能等待对癌症的透彻理解,今年将有325000美国人死于癌症,他们不能等待;我们没有必要为了在癌症治疗方面取得巨大进展而追求在基础研究领域对所有问题都获得圆满的答案。在人类医学史上有很多案例,人们往往在获得成功疗法以后几年、几十年甚至几个世纪才理解治疗机制,比如牛痘、洋地黄、阿司匹林都是如此。”
可是他在这场争论中失败了。
追求知识成为终极目标
今天癌症研究已经细分为许多专业领域,精确计算政府从1971年至今在癌症研究领域投入的经费几乎已经不可能。不过从国家癌症研究院以及其上级单位国家卫生研究院每年得到的经费以及大制药企业投入的研发费用、私人捐助等等,仍然可以估算出总的投入。从1971年以来,投入癌症研究的总经费大约是2000亿美元,通货膨胀因素已经扣除。
毫无疑问,投入的庞大经费已经换来了大量的知识。科学家们已经了解(或是他们认为已经了解)健康细胞成长、分裂、凋亡的几乎所有生物化学步骤,以及指导这些过程的基因。他们还了解这些由基因启动的过程在癌细胞里是如何变得乱七八糟的。
根据国家癌症研究的在线数据库PubMed,癌症研究领域的研究论文已经有156万篇!这些论文发表在数百种学术期刊。许多论文还在每年召开的各种国际学术交流活动中发布。
不过,一些重要的东西失落了。追求知识本身成了终极目标,而不是成为追求真正的终极目标的手段。研究领域变得越来越窄,以至于那些试图系统地看待癌症、试图从总体把握癌症或是试图用全新方法研究癌症的科学家们反而得不到研究资助。
举例来说,国家癌症研究院的主要资助机制被称为RO1,2003年获得该项资助的项目得到的经费平均是338000美元。要获得该项资助相当容易,每3项申请中就有一项获得资助。不过这笔款项大多用来资助那些专注于癌细胞或其它组织中某个特定遗传或是分子机制的项目。研究领域越窄越容易获得资助。M.D.安得森癌症医院负责科研管理的副院长里沃纳德评论说:“这种激励机制同目标不匹配,如果目标是癌症治疗,那么就不应当资助那些难以发表有影响论文的小课题。”他的观点代表了相当一部分人。
伊萨是里沃纳德的同事。他说得更明白:“如果你把某个基因做了细微改变,发现在实验小鼠身上的癌瘤发生较大变化,于是你在科学或是自然周刊这样最出名的学术期刊上发表相关论文,你有名了,资助就来了。你去看那些论文,80%%是以小鼠、果蝇或是蛆虫作为实验对象。那么什么时候那里才会有人类癌症的论文呢?”
事实确实如此。对PubMed在线数据库的检索表明,有150855篇论文是以老鼠为实验对象的。猜一猜有多少小鼠论文是真正对癌症治疗有影响的?非常非常少。实际上,如果你试图理解抗癌大战是如何走错方向的,那么实验小鼠是一个非常好的起点。
小鼠模型的误区
不同的生物物种之间是有关联的。这种关联突出体现在DNA里。人类基因组分享了地球上生命的许多神奇的基因密码。一种小鼠基因也许同一种人类基因非常相似。正因如此,对癌症研究而言,这里同时存在着诱惑与挫折。
特定基因变异会导致细胞增生,增生失去控制,蔓延到其它本不该有这种细胞的组织,并且拒绝在适当的时候凋亡,这就是癌症。所以研究首先就是要弄清楚基因变异的分子机制,其次,寻找药物以阻断这种机制。
兰德是有“核苷酸王子”美名的科学家,他勾画癌症治疗的生物学途径就像是他指点你去附近的星巴克咖啡馆一样容易。“这里只有3万个基因,这些基因的作用是有限的,癌症形成机制的种类也是有限的,可能一共有100种癌症形成机制,100种就是100种。”
他接着解释,我们需要协调合作,通过寻找小鼠的致癌基因,并分离这些成癌机制,试验能够杀死变异细胞的药物,最终发现癌细胞的致命弱点。合理的癌症治疗方法就是发现癌细胞每一种新变异的致命弱点。
这一方法的原理是对的。但是这一方法自身也许同样存在致命弱点。小鼠的某个基因也许同某个人类基因相似,但是其它基因同人类基因相比也许差别很大。
这一事实大概被许多采用小鼠模型的研究人员忽略了。麻省理工学院生物学教授温伯格曾因发现人类第一个致癌基因及第一个人类抑癌基因而获得国家科学奖。他指出:“人类癌症研究一个最常用的方法是把人类癌细胞放在培养皿培养,然后移植到实验小鼠身上,这是一种免疫机制被抑制的实验小鼠,使肿瘤生长,然后对异种移植肿瘤试用各种药物,其中可能有能够治疗人类癌症的药物。这被称为临床前模型。”
温伯格解释说:“实际上十多年甚至二十多年来,大家都知道,对于预测药物在实际人类癌症治疗的作用,这种人类癌症临床前模型的预测效果非常差。”换句通俗的话就是:能治小鼠身上异种移植癌的药物,大多治不了实际癌症患者的癌。
温伯格的结论很明确:“这是癌症研究长期面临的一个基本问题。从治疗角度看,人类癌症的临床前期模型已经臭名昭著。”
为什么会发生这种情况?原因还是前面所说,癌症擅长变异,在培养及异种移植过程中,癌细胞早已变异。比如你采集某位病人的肺癌细胞,培养以后异种移植,你就获得了一个肺癌的临床前期模型。实际上这一模型已经不再是原始肺癌模型,因为人类肺癌已经有上百种变异。
可是99%%的研究人员仍然在使用这种癌临床前期模型。这是为什么?基因技术公司(Genentech)的一位研究人员VishvaDixit一言道破原因:这一方法简单易行。如果药物作用有效,肉眼就能看出移植肿瘤在缩小。制药公司内部对这一问题都有共识,但是迄今没有采取措施去纠正。按照温伯格的说法,大量的经费因为这一临床前期模型而被浪费。
更令人沮丧的是大量可能对人类癌症有效的药物因为这种临床前期模型而被淘汰。对小鼠身上移植肿瘤有效的药物对人类实际癌症大多无效,那么反过来,对小鼠移植肿瘤无效的药物就可能对人类癌症有效。而由于药物筛选判别标准是小鼠模型,所以对小鼠无效的药物首先被淘汰。
既然所有人都清楚问题所在,那么为什么没有采取改进措施?
理由也很简单。温伯格说,第一,现在没有能够替代可怜的小鼠的模型;第二,问题出在管理部门,美国食品药物管理局已经形成一种惯性,这种小鼠模型已经成为判别药物疗效的黄金标准。
抗癌大战:人类如何才能获胜?(下)
先有鸡还是先有蛋
这里又出现先有鸡还是先有蛋的悖论。到底是先有美国食品药物管理局的药效判别标准,还是先有那些药厂都广泛应用的小鼠模型?
不论如何,食品药物管理局还是关注药物的临床实验结果。食品药物管理局把肿瘤缩小称为肿瘤退化。药物疗效的一个直观结果是瘤体缩小,能够看到瘤体缩小是令人兴奋的,然而肿瘤退化对于预测癌症进程却是一个很差的指标,令人悲观的事实是肿瘤退化并不能改善癌症患者的生存概率。因为瘤体缩小并不等于没有癌细胞转移,实际上大部分癌症病人最终死于癌转移。
如此说来,癌转移应当是研究人员关注的重大课题。然而根据财富杂志的调查,从1972年至今,在国家癌症研究院的资助项目中,只有不到0.5%%的项目是研究癌转移的。去年国家癌症研究院的资助项目有8900个,其中92%%甚至根本没有提到癌转移。
两年前,一位功成名就的研究人员向国家癌症研究院提交一份建议书,建议研究癌转移过程产生的正常基因功能的变化(epige鄄netics),并同原发癌进行比较。到现在为止,这位研究人员已经第三次提交这份建议。他说:“我的意思是我们对此确实一无所知。可是我却无法说服有关方面资助这一研究。”
费得勒对此的解释很直白:“这太难。研究人员并不会因为从事艰难的研究而得到资助。那些审查资助项目的官员更喜欢资助那些目标集中、单一的项目,例如这是一种我要用的抗体,那是我需要的什么什么,于是钱下拨。”
另一方面,癌转移属于重大课题,这一器官一级的现象可能包括数十种进程。癌转移很复杂,变数太多,因此研究人员要创建一种能够重复的实验是很难的。但是这正是我们需要的研究。而按照温伯格的说法,研究人员为了获得资助,总是绕开这一课题,去做那些比较简单、能够重复结果的实验。不幸的是,“数据的积累给人们一种错觉,以为他们在做很有意义的事情。”这是温伯格的结论。
这种数据积累的驱动力源自指导药物开发的政府部门存在的核心问题。食品药物管理局的使命是要确保某种药物在上市之前是安全有效的。这样,FDA的官员们要看到这种药物在试验中有效的过硬数据。可是,很难看到那种最初阻止癌转移的“活力”。也许存在某些生物标记物,比如某些蛋白质,能够告诉我们癌细胞开始扩散到其它组织。可是迄今为止,我们还不知道这类物质是什么。
所以制药公司很自然地放弃解决癌转移问题(这是癌症患者的杀手)这样的重大目标,而把目标定位在肿瘤缩小(这并不能拯救癌症患者)。
尽管存在严重问题,还是有数十种药物获得FDA批准。同时有很多药物没有获得批准,于是FDA受到批评,人们指责FDA是在延误抗癌大战。不过问题与其说在仲裁者,不如说在参与者。因为许多能够导致肿瘤缩小的新药并不能产生比标准疗法更好的疗效。或者就干脆如FDA负责抗癌药物的主任里克・帕兹德(RickPazdur)所说:“那是疗效,真是愚蠢!我们面临的一个主要问题是要同这种不明确的疗效打交道。”如果确实有效,食品药物管理局会优先审批或是加速批准。
去年8月,两位意大利药理学家在英国医学月刊(BritishMedicalJournal)上发表论文,对1995年-2000年间在欧洲上市的12种抗癌新药的疗效同相关标准疗法进行比较,他们没有发现这12种新药有任何实质性的优越之处:患者生存率没有提高,生活质量没有改善,安全性也没有改进。而所有这些新药的价格却大幅上升,比传统药物的价格高几倍,其中一种新药甚至比“旧药”贵350倍。
为什么抗癌新药令人失望
药物开发的模型存在缺陷。肿瘤缩小令人困扰。专注于单个细胞机制的研究却忽略了器官整体正在发生的变化。所有这些问题到了临床试验的时候便面临考验。临床试验分为三期,受到严格控制,专门用来测试新药以及其它医学疗法在人体的疗效。临床试验是新药从研究通往审批合格的必由之路,迄今为止还没有发现任何从事癌症药物研究的人员不被临床试验折腾得怒火中烧、垂头丧气。
2003年2月,一批名声显赫的癌症研究中心主任们得出结论:临床试验是长期而艰巨的,由于管理规章严格而成为负担,如果不进行重大改革,提供更多的资源,临床试验体系“将仍然是低效率、不能及时反应、过于昂贵的。”
几乎所有癌症患者都知道癌症新药临床试验不会带来希望。事实上97%%的成年癌症患者都不愿参与癌症新药临床试验。
临床试验存在两大问题。第一是试验周期长,成本高昂,资助临床试验的通常是制药厂商,这些厂商把测试那些有可能通过FDA评审的药物放在至高无上的位置。因为不论如何,这些公司都是公开上市的,股东们要求投资有回报。所以制药公司的目标不是专注于突破性的疗法而是对现有药物逐步改良。临床试验过程并不鼓励冒风险或是提倡可能在医药领域获得重大发现的开拓性方法。临床试验体系不鼓励大胆的全新思维。一种新药的开发周期通常长达12-14年,平均开发成本高达8.02亿美元,这些经常被公布的数字也不鼓励真正的创造精神。
更糟糕的是,临床试验体系迫使制药公司在最为危重的癌症病人身上试验那些最有希望的新药,因为这样更容易看到诸如肿瘤缩小这样的效果,可是几乎不可能治愈患者。因为癌症晚期,癌细胞通常已经大范围扩散,而且由于基因变异,癌瘤已经过度溃烂。这样如果一种新药可能对早期癌症患者有效,却没有机会在临床试验中得到证实。
临床试验体系存在的第二大问题的后果更为严重。临床试验的目标有误,其目标不是为了治病救人,而是为了实施“适当”的科学。这并不是说参与临试的患者没有得到应有的治疗,通常参与临试的患者都得到很好的治疗。可是临床试验之所以实施的主要理由是要证实一种假说:疗法X是否优于疗法Y?而时常出现的结果是,经过长期、令人费解的过程,收集到的数据却没有什么意义。比如你耗费10年以上时间发现一种新药,这种新药与现有疗法相比,缩小癌瘤的程度平均增加10%%,这种新药会对多少癌症患者有益呢?
以两种今年2月才获批准的治疗肠癌的新药为例:Erbitux及Avasteen。这两种药物的临床试验都用了好几个月招募参与临试的癌症患者。参与临试的医师要按照事先准备、读起来费劲的协议管理药物,一路收集数据。
经过数年临试,最终数据出台。在肠癌化疗药物中加入Avasteen,参与临试的400名晚期肠癌患者的生存期平均延长了4.7个月,肿瘤学家们认为这一数字有实质意义,因为晚期结肠癌或是直肠癌患者的生存期平均少于16个月。
Erbitux又怎么样?虽然这种药物确实能够缩小癌瘤,但是它却无助于延长晚期肠癌患者的生存期。确实有患者用此药以后效果不错,可是对参与临试患者的统计表明,这种药物对延长患者生存期无效。虽然如此,Erbitux仍然获得上市许可,主要用于其它疗法均无效的第三系列治疗。一周剂量的Erbitux耗资2400美元。
要记住,临床试验耗费数年时间,先后有数千名患者参与三期试验,收集了数以吨计的数据,耗资巨大,最后发现了临试医师及研究人员在早期临床试验中已经得出的结论。无论这两种药的哪一种,都无法拯救今年将要死于结肠癌及直肠癌的57000名美国患者中哪怕少数人的生命。
肺癌靶向药物Iressa是AstraZenecca开发的一种采用最新生物技术的药物,它干扰癌细胞中的一种分子信号。可是没有临床试验数据表明这一药物能够减轻患者症状或是延长生存期,如同AstraZenecca公司新闻稿上公司介绍那段话中声称的疗效。尽管如此,FDA还是在去年批准该药作为最后的治疗手段用于一种类型肺癌的治疗,指出有10%%肺癌患者的肿瘤在使用该药以后缩小。
Dana-Farber的布鲁斯・约翰森(BruceJohn鄄son)总结说:“非常聪明的人,用了很多钱,在世界范围对一万多名肺癌患者开展临床试验,测试这些分子靶向药物。AstraZenecca公司试验了Iressa,Isis制药公司以及EliLilly公司测试了名为Isis3521的药物。几家不同的公司总共投资了数千万美元,结果是个大零蛋。”
有一种靶向药物显然不是大零蛋,这就是Novartis公司开发的Gleevec。这种新药不仅能缩小肿瘤,而且能够拯救生命。这种新药治疗一种不常见的白血病CML有奇效,治疗一种更为罕见的胃癌GIST疗效也很好。早期的临试报告称Gleevec对其它三种癌症也不同程度有效。Gleevec的成功被人们用来作为证据,证明这些年来抗癌策略是正确的。
可是就是Gleevec也不能支持上述论点。首先,CML不是复杂的癌症,单个基因变异导致关键信号机制出错,Gleevec巧妙地阻断了致命的信号。而大多数常见的癌症则是有5-10种机制出错。其二,甚至“简单”的癌症也变得机敏起来,由于患者必须终生服用Gleevec,癌细胞在药物作用下变异,绕开Gleevec阻断的信号,由此产生抗药性。
所以癌症比心脏病更为令人沮丧,这不足为奇。
鲍勃・科恩(BobCohen)是Genentech公司商业诊断产品部门的高级总监,他指出,用一种药物如果不能完全摧毁肿瘤,那么“癌细胞的非一致性就会演化,并说:‘就那么个破玩艺儿可骗不了我。’突然你会发现复杂性以平方甚至立方的速度上升。这就是我们的处境。”正因如此,对付癌症的唯一机会是早期发现,并从多个角度开展全面攻击。
那么用3种、4种甚至5种药物联合攻击,或是像治疗艾滋病那样用多种化合物组成鸡尾酒疗法控制擅长变异的艾滋病病毒那样对付癌症,当然是一种办法。事实上我采访的临床医师及科学家都相信新一代抗癌药物应当采用类似的方法。可是,癌症领域的习惯势力却使这种方法几乎不可能实施。
在临床试验中联合应用几种未经批准的化合物会产生一系列法律、法规问题,制药公司会望而却步。制药公司需要FDA批准他们开发的新药用于临床。如果2种或3种以上药物联合使用,难以确认哪一种药物有效、哪一种无效,或是哪一种药物应当对某种副作用负责。
休斯顿M.D.Anderson医院的Kleinerman是一位临床试验医师,她曾经3次尝试用不同制药公司的药物联合治疗参与临床试验的儿童癌症患者。第一次,由于临床试验时间太长,参与临床试验的一家新兴生物制药公司倒闭了;第二次,由于律师们纠缠于责任问题,最后两家制药公司撤出;第三次最糟糕。联合使用两家制药公司的新药已经激发免疫系统针对骨肉瘤癌细胞展开更有效的战斗,骨肉瘤是一种儿童的骨癌。同两家制药公司律师协商的结果却是不可能。因为两家公司都要对两种药物联合处方拥有独家权利。
改变我们对于癌症的看法
也许令人感到奇怪,我们在与癌症抗争中的失败,或者更重要的是我们未来征服癌症的潜力同癌症的定义有关。
大约2400年前,希腊名医希波克拉茨把癌症描述为一种会扩散并像“蟹钳”一样侵犯身体其它部分的疾患。现代医学教科书也对癌症有类似的描述,癌细胞必定侵犯身体其它部位。
Dartmouth医学院教授迈克尔・斯伯恩(MichaelSporn)认为这一定义毫无意义。他认为,癌症的发生比癌细胞侵犯其它器官要早得多。所以他相信能够有最佳策略限制癌症的发展。积极寻找那些在我们身上隐藏多年的火种,在它们蔓延成火灾之前扑灭它们。就是从一开始就设法阻止癌症发展到致命的阶段。
斯伯恩在国家癌症研究院已经工作了30多年。多年来他一直强调,癌症不是已经长大的癌瘤,癌症是一个过程,称为癌发生过程(carcinogensis)。癌症是一种多阶段的疾病,其间细胞发生多次变化,在其发展过程中可能有很长的潜伏期。
这样,只要我们能在癌发生过程的早期特别是在某些损害发生的关键时刻进行干预,就可能中止癌发生进程。要做到这一点,医学界必须抛弃那些认为患者在癌发生初期是“健康”的,无须治疗的观念。只要患者处于癌发生过程,他们就不是健康的。
这看起来有点牵强。可以这么考虑:我们已经采用相同策略预防了数百万心脏病及脑中风发作。心脏病不是从心肌梗塞开始的,心脏病开始于更早的阶段,血液中胆固醇及血脂高并导致动脉粥样沉积,我们针对这些症状进行治疗;脑中风也不是从脑血栓开始,而是从高血压开始的,所以我们通过改变生活方式及药物进行治疗。斯伯恩认为:“心脑血管疾病当然不如癌症复杂,但是原则是一样的。人们总是为治愈癌症的目标所困扰,却总是找不到奇迹般的癌症根治术。恕我直言,由于忽略了预防癌症的手段,这些人显得有点自私。”
令人惊讶的是,这套理论现在就能付诸实施。癌前期的细胞变化表明,多种癌症的发生进程已经开始;许多癌前期变化相对容易被发现并去除,还有一些癌前期变化可以通过现有药物或是疗法使之逆转。
一个完美的例子就是宫颈涂片检测(Papsmear),这一方法能够发现宫颈部细胞的癌前期变化。采用这一简单方法,宫颈癌死亡率从上世纪50年代以来降低了78%%-79%%;在宫颈涂片检测没有推广的国家,宫颈癌是妇女的第一杀手。
同样的方法可以用于结肠癌。虽然不是所有的肠息肉都会发展成癌,但是这是结肠癌发展过程中必然的一步。显然,医生们已经在做类似的检测,以期发现一些癌前期变化。不过他们需要在这方面做的工作远比已经做的要多得多。
如何赢得抗癌大战
美国要赢得抗癌大战,癌症医学界及学术界必须联合作战,针对癌症发动攻击。医生与科学家们已经拥有足够的知识实施33年前西德尼・法伯(SydneyFarber)期待的行动:像一支军队一样联合作战,而不是单兵各自为战。
国家癌症研究院应当率先变革,改变它资助癌症研究的方式;消除由RO1资助方式产生的癌症文化(RO1资助方式产生了大量重复、基于你有我也要有原则的研究项目),转而资助专注于重大课题的合作研究项目。国家癌症研究院已经设立这样的资助方式,如SPOREs(Shortforspecializedprogramsofresearchex鄄cellence)项目经费,这样的资助方式能够吸引不同领域的研究人员开展合作,从多个方面对癌症开展研究。不过国家癌症研究院在一个季度里资助个别研究项目的经费是SPORE项目经费的12倍以上。国家癌症研究院应当停止充当ATM取款机,把纳税人的钱用于重大课题研究,例如如何防止癌转移,或是建立更为有效的癌临床前期模型。
同时,国家癌症研究院应当致力于通过血检、尿检或是改进的分子成像技术(PET或是CT扫描)以发现能够预测癌症发展进程的生物标记物,为癌症患者提供早期根治癌症或是控制癌症的机会。说到癌症预防,按照国家癌症研究院的统计,只要实施全民戒烟,就能减少30%%的癌症死亡病例。我所采访的所有研究人员都提到了这一过于显然的观测结果。
当然这不是百万美元的项目,这是以十亿美元计算的项目。可是我国已经投资数十亿美元于癌症研究,更何况我国每年还要花费640亿美元用于癌症治疗。为了使资源的转移更为畅通,国会应当把联邦政府指挥抗癌大战的机构从5个削减到1个,由国家癌症研究院统一管理癌症研究,而不用五角大楼等部门参与。
同等重要的是,食品药物管理局作为抗癌的指挥机构,应当同法规制定者一起共同改革药物试验及审批机制,大大加快向患者提供哪些药物有效、哪些无效等重要信息的进程。如果多种药物联合使用带来可能治愈多种癌症的希望,我们应当设法打破法律限制,采取措施激励制药厂商在时间较短的临床试验中试验多种药物联合处方。这样的试验应当由国家癌症研究院提供资助,这一机制同单项药物审批机制完全不同。如果确有证据表明几种药物联合使用能够明显延长癌症病人生存期,那么应当启动FDA的加速审批机制。
(克里夫顿。利夫 胡永生摘译)
|
